見出し
今日の勉強内容
昨日に引き続き、MEC 血液のテキストを復習していました。
今日勉強していた内容が白血病だったのもあると思いますが、血液疾患は難しい。機序や分類が複雑なうえに、治療法も似たようなものが多い。そもそも血液という見えづらいものを扱っているので、理解するのが難しいという側面があると思います。
そしてさらに現場だと、疾患名も薬剤名も全部英語なのでカルテが暗号文化してしまうという難しさがあるのです…去年のポリクリ中、Ara-Cとシタラビンとキロサイドが全部一緒の薬であることを知って、衝撃を受けた記憶があります。
そんな血液内科ですが、基本的に薬で治療をしていく科なので化学療法に興味がある人は良いんだろうなーと思います。あと理論派の人向きな気がする(自分はムリ)
以下は今日の勉強ノート
§4 白血病
骨髄において白血病細胞(CLL以外は芽球)が腫瘍性増殖をきたした疾患。末梢血中にも白血病細胞が出現する。
急性白血病と染色
- MPO染色陽性(黄褐色):M0/7を除くAML
- 特異的エラスターゼ染色陽性(青色):M1〜M4(好中球系)
- 非特異的エラスターゼ染色陽性(茶褐色):M4・M5(単球系)
- PAS染色陽性:M6
※M4は好中球・単球のどちらにも分化できるため特異的/非特異的エラスターゼ染色で陽性となる(下図参照)
白血病と染色体異常
- M2:t(8;21)
- M3:t(15;17)
- L3(バーキットリンパ腫/白血病):t(8;14)
- CML:t(9;22)
腫瘍崩壊症候群
化学療法や放射線療法によって、白血病細胞が大量に破壊されると細胞内の成分が血中に流出して生じる症候群。
症状としては高尿酸血症・高カリウム血症・高P血症などが出現する。予防としてフェブキソスタット(尿酸産生抑制薬)を使用する。
AML(急性骨髄性白血病)
骨髄系芽球細胞の腫瘍性増殖による疾患。
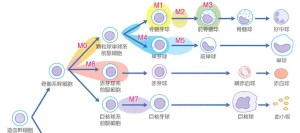
FAB分類においてはどの分化段階の細胞が異常増殖をきたしているかによって、M0〜M7に分類される。
source:病気がみえる vol.5 血液 第1版(メディックメディア)
WHO分類ではさらに、染色体異常や治療関連AML(抗癌剤の副作用による二次的なAML)を加えて分類する。
・M5
歯肉腫脹、血中リゾチーム増加や検査所見における非特異的エラスターゼ染色陽性、核の切れ込みなど特徴的な所見を持つ
治療
・基本
- 寛解導入療法:AraC(シタラビン)+IDR(イダルビシン)/DNR(ダウノルビシン)
- 寛解後療法:HDAC(大量シタラビン)療法
予後不良例や難治性/再発例では造血幹細胞移植を考慮する。
また難治例・再発例では抗CD33モノクローナル抗体+抗腫瘍抗生物質であるGOの投与も行われる。CD33はAMLの白血病細胞の約80%に発現しているため、白血病細胞特異的に作用すると考えられている。
・M3(APL)の場合
RARαは正常ではコリプレッサーの結合による転写活性制御を受けており、レチノイン酸により結合が解除されることで前骨髄球から骨髄球への分化が生じる。
しかしAPLではt(15;17)の染色体異常のため、キメラ蛋白であるPML/RARαが形成される。この蛋白はコリプレッサーとの結合性が高くレチノイン酸による分化促進を受けないため、前骨髄球以降へ分化することができない。
上記のような機序であるため治療には分化誘導療法としてATRA(コリプレッサーを外す能力が強い)が用いられる。
また白血球数が多い場合(≧3000)は、ATRAによって分化誘導された好中球がサイトカインを放出してレチノイン酸症候群と呼ばれる副作用を生じる。そのためこの場合はアントラサイクリン系薬剤やシタラビンを併用して腫瘍細胞の数を減らすことが行われる。
再発例では亜ヒ酸を用いる。
ALL(急性リンパ芽球性白血病)/LBL(リンパ芽球性リンパ腫)
リンパ系前駆細胞(リンパ芽球)の腫瘍性増殖により生じる疾患。
分類にはWHO分類が用いられることが多く、B細胞系腫瘍かT細胞系腫瘍かで大まかに分けられる。骨髄や末梢血を中心として増殖している場合をALL、リンパ節を中心して増殖している場合をLBLと呼ぶ。
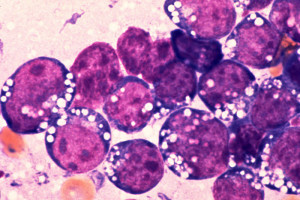
バーキットリンパ腫/白血病は成熟B細胞系腫瘍であり、リンパ芽球ではないが臨床像が似ているためALLとして扱われる。骨髄血塗抹標本で脂肪空胞を認めるのが特徴的。
source:症例4-2, Giemsa ×500.JPG
治療
- 寛解導入療法:VCR(ビンクリスチン)・PSL(プレドニゾロン)を用いたVP療法+アントラサイクリン系薬剤であるDNR/DXR。さらにL-アスパラキナーゼやシクロホスファミドを加える。
- 寛解後療法:上記で用いなかった薬剤を用いた多剤併用療法
予後不良群では造血幹細胞移植を考慮する
CML(慢性骨髄性白血病)
造血幹細胞レベルの未分化な細胞で染色体異常t(9;22)が生じ、その結果生じるキメラ蛋白BCR/ABLチロシンキナーゼは恒常的に活性化されていることから異常増殖をきたす疾患。
慢性期には脾腫や肝腫を認め、やがて移行期をへて急性転化を起こす。この移行は染色体付加異常が加わることによって生じ、検査値的にはNAPスコアの上昇がみられる。
※CML→ALLへの急性転化とALLはどちらもフィラデルフィア染色体が陽性となるが、好中球にBcr-Ablが存在するかをFISH法で調べれば鑑別できる。(もちろん病歴も参考になる)
CLL(慢性リンパ性白血病)/SLL(小リンパ球性リンパ腫)
成熟小型リンパ球(B細胞性)の腫瘍性増殖による疾患。しかしなぜかT細胞マーカーであるCD5が陽性となる。CLLは骨髄や末梢血を中心に増殖が生じ、SLLはリンパ節を中心に増殖が生じる。
※白血病なのに芽球ではない!
日本では白血病の2〜3%と稀だが、欧米では20〜30%と比較的多い。
正常な抗体産生が抑制されることから液性免疫・細胞性免疫は抑制される。しかしCD5陽性B細胞は自己抗体の産生に関与することから、Ⅱ型アレルギー疾患であるAIHAやITPを合併することがある。
体重減少や倦怠感などの症状を伴っているとき、または急激なリンパ球増加があるときは治療対象となり、フルダラビンやリツキシマブが用いられる。
CMLと違って急性転化することはないため、無症状なら積極的な治療は行わない。
ATLL(成人T細胞白血病/リンパ腫)
レトロウイルスであるHTLV-1の感染により生じるT細胞腫瘍。CD4陽性成熟T細胞が腫瘍性に増殖する
症状
細胞性免疫の低下から、ツベルクリン反応の陰転化や易感染性を呈する。またT細胞系腫瘍なので、皮膚浸潤をきたしやすい。
分類と治療
くすぶり型・慢性型・リンパ腫型・急性型に分類される。
くすぶり型や慢性型ではCLLと同じく経過観察が原則。
急性型やリンパ腫型ではCHOP療法(シクロホスファミド+ヒドロキシドキソルビシン+オンコビン+プレドニゾロン)にG-CSFを追加した治療が試みられるが予後は不良。
§5 骨髄の機能亢進と低下
骨髄増殖性腫瘍:慢性骨髄性白血病(CML)・真性赤血球増加症(PV)・本態性血小板血症(ET)・原発性骨髄線維腫(PMF)
真性赤血球増加症(PV)
JAK2遺伝子の変異(95%)により多能性造血幹細胞レベルでの腫瘍性増殖が生じる
症状・検査
(名前の割に)赤血球以外の系統の血球も増加するため、汎血球増加となる。血液粘稠度が亢進することから血栓症をきたしやすい。また好塩基球増加による抗ヒスタミン血症(皮膚掻痒感)も生じる。
赤血球は増加するが、相対的に材料が不足するためMCV低値となる。好中球も増加するためNAPスコアは高値となる。
治療・予後
治療は対症療法的な瀉血・抗血小板薬など。血栓症の既往がある場合、血球制御のためにヒドロキシウレアを使用することもある。JAK2キナーゼ阻害薬も用いられる。
15%の患者で診断後平均10年で消耗期と呼ばれる骨髄線維症へ移行する。
本態性血小板血症(ET)
多能性造血幹細胞レベルでの腫瘍化が生じる。JAK2遺伝子の変異は50%に生じている。
末梢血中では血小板の増加や巨大血小板を認める。骨髄中では巨核球が増加する。血小板増加により血栓症状をきたすことが多いが、血小板の機能が低下しているため出血症状をきたすこともある。
治療はPVと同じく対処療法+ヒドロキシウレア(+JAK2キナーゼ阻害薬)
原発性骨髄線維症(PMF)
造血幹細胞レベルで生じた遺伝子異常により、巨核球を中心とする異常増殖が生じる。やがてサイトカインの関与を経て線維芽細胞が活性化され骨髄の線維化へと到る。
この疾患もJAK2遺伝子変異を50%の症例で認める。
骨髄線維症には原発性のものと、CML・MDS・PVなどに続発するものがある。
症状
巨核球の異常により、巨大血小板を生じる。
骨髄での造血が行えなくなることから、脾臓での髄外造血が始まり巨脾をきたす。髄外で作られた血球は涙滴赤血球などの形態異常を生じており、また脾臓では未熟な細胞も放出されるため末梢血中に芽球の出現(白赤芽球症)を認める。
治療
造血を促す目的での蛋白同化ステロイドの他、ヒドロキシウレアやサリドマイドも用いられる。
また根治的治療として造血幹細胞移植がある
※分類上は骨髄増殖性疾患とはいえ、結果的に骨髄が線維化して造血に問題が生じてくる疾患なので、”造血を促す”ために蛋白同化ステロイドや造血幹細胞移植が行われる。
再生不良性貧血(AA)
末梢血での汎血球減少と骨髄の低形成を特徴とする症候群。特発性のものと、薬剤性(クロラムフェニコール)や化学物質(ベンゼン)などによる二次性のものがある。またPNHに伴うものもある
特発性は造血幹細胞に対する自己免疫反応が原因とされるが、詳細は不明。
分類・治療
網赤血球・好中球・血小板の数で重症度が分類される。どのステージにおいても支持療法としての輸血やG-CSF投与は行う。
- ステージ1・2:造血を促すために蛋白同化ステロイドが用いられる。
- ステージ3以上:自己免疫反応が関わっているとされるため、ATG(抗ヒト胸腺グロブリン)やシクロスポリンを用いた免疫抑制療法が行われる。
重症例で40歳未満の場合は造血幹細胞移植も行われる。ただしHLA一致同胞でないと予後はあまり良くない
赤芽球癆
赤芽球やその前駆細胞の障害により、網赤血球・赤血球の低下をきたす疾患。急性の原因としてパルボウイルスB19感染(赤芽球前駆細胞に感染)が、慢性の原因として胸腺腫との合併が知られる。
治療には免疫抑制療法としてシクロスポリンやステロイドが用いられる。
※治療方針も類似しており、「赤芽球系オンリーの再生不良性貧血」と考えると解りやすい