日本皮膚科学会 皮膚科専門医試験 令和1(2019)年度の解答解説を作成しました
見出しから各問題へ飛べます
誤字脱字ご意見などあればコメント・右のフォーム・Twitterなどでご連絡ください
- 問題出典:試験問題(過去問題) |公益社団法人日本皮膚科学会 (問題・写真はリンク先で確認下さい)
- 参考文献:あたらしい皮膚科学 第3版、皮膚科学(マイナー) 第10版でカッコ内は選択肢番号、その他は問題末に各自記載
※本記事で参考にしたのは皮膚科学 第10版ですが、11版が出ているので上記リンクは新版です
2020年度の解答・解説は下記
-

-
令和2(2020)年度 皮膚科専門医認定試験 過去問 解答解説
続きを見る
見出し
- 1 令和1年度(2019年度) 皮膚科専門医試験 過去問 解答解説 選択問題1〜30
- 1.1 選択問題1:解答 5
- 1.2 選択問題2:解答 3
- 1.3 選択問題3:解答 1, 2, 3
- 1.4 選択問題4:解答 3
- 1.5 選択問題5:解答 1, 4(現在は4のみ)
- 1.6 選択問題6:解答 3
- 1.7 選択問題7:解答 2, 4
- 1.8 選択問題8:解答 3
- 1.9 選択問題9:解答 4
- 1.10 選択問題10:解答 1
- 1.11 選択問題11:解答 3, 4
- 1.12 選択問題12:解答 5
- 1.13 選択問題13:解答 5
- 1.14 選択問題14:解答 3, 4
- 1.15 選択問題15:解答 2
- 1.16 選択問題16:解答 3
- 1.17 選択問題17:解答 1, 3, 4
- 1.18 選択問題18:解答 3, 4, 5
- 1.19 選択問題19:解答 1, 2
- 1.20 選択問題20:解答 1
- 1.21 選択問題21:解答 4, 5
- 1.22 選択問題22:解答 4
- 1.23 選択問題23:解答 2
- 1.24 選択問題24:解答 1
- 1.25 選択問題25:解答 5
- 1.26 選択問題26:解答 5
- 1.27 選択問題27:解答 4
- 1.28 選択問題28:1, 2, 3
- 1.29 選択問題29:解答 2
- 1.30 選択問題30:解答 3, 4
令和1年度(2019年度) 皮膚科専門医試験 過去問 解答解説 選択問題1〜30
選択問題1:解答 5
特発性後天性全身性無汗症の診断基準では、病理組織像で汗腺周囲の"リンパ球浸潤"が含まれる→5
特発性後天性全身性無汗症(AIGA)の診断基準
- A:明らかな原因なく後天性に非髄節性の広範な無汗/減汗(発汗低下)を呈するが,発汗以外の自律神経症候及び神経学的症候を認めない.
- B:ヨードデンプン反応を用いたミノール法などによる温熱発汗試験で黒色に変色しない領域もしくは サーモグラフィーによる高体温領域が全身の 25% 以上の範囲に無汗/減汗(発汗低下)がみられる.
A+B をもって AIGA と診断する.
参考項目
- 発汗誘発時に皮膚のピリピリする痛み・発疹(コリン性蕁麻疹)がしばしばみられる.
- 発汗低下に左右差なく,腋窩の発汗ならびに手掌・足底の精神性発汗は保たれていることが多い.
- アトピー性皮膚炎は AIGA に合併することがあるので除外項目には含めない.
- 病理組織学的所見:汗腺周囲のリンパ球浸潤,汗腺の委縮,汗孔に角栓なども認めることもある.
- アセチルコリン皮内テスト又は QSART で反応低下を認める.
- 抗 SS-A 抗体陰性,抗 SS-B 抗体陰性,外分泌腺機能異常がないなどシェーグレン症候群は否定する.
引用:特発性後天性全身性無汗症診療ガイドライン 改訂版.自律神経 52 : 352―359, 2015.
-

-
特発性後天性全身性無汗症(AIGA) 診断基準・重症度分類
続きを見る
- 1・3. 腋窩の発汗や掌蹠の精神性発汗は保たれる
- 2. AIGAのうち、特発性純粋発汗不全(IPSF, AIGAの9割を占める)では血清IgE値の上昇を認めることがある
- 4. 発汗時の皮膚のピリピリする痛み・発疹(コリン性蕁麻疹)がしばしば見られる
- 5. 病理組織では汗腺周囲の"リンパ球"浸潤がみられ、シクロスポリンが有効であったという報告もある
- 参考書籍:あたらしい皮膚科学 第3版 p363(4)
- 参考書籍:皮膚科学 第10版 p738(4)
- 選択肢2の参考:特発性後天性全身性無汗症(指定難病163) – 難病情報センター
IgE上昇と汗腺周囲のリンパ球浸潤については比較的稀な所見という報告もある:新・皮膚科セミナリウム 特発性後天性全身性無汗症 日皮会誌:131(1), 35-41, 2021
※ただし本問出題より後の論文
関連:AIGAについては複数回出題あり、上記記事参照
選択問題2:解答 3
尋常性乾癬に対して抗IL-17抗体製剤治療中に白苔が生じている
抗IL-17A抗体製剤(セクキヌマブ・イキセキズマブetc)の有害事象として、真菌感染がある
舌の白苔(口腔カンジダ症)を認めるも乾癬自体の悪化はないため、生物学的製剤の投与を続けつつ抗真菌薬外用(フロリード®ゲルなど)にて対応する→3
カンジダ感染が遷延する場合には、定期的なβ-Dグルカン測定も推奨されている
- 1. 細菌感染である黄色ブドウ球菌感染症(IL-17阻害で生じやすい副作用)では抗菌薬投与を行う
- 2・5.生物学的製剤:乾癬自体の悪化はないため、薬剤変更(抗TNF-αやPDE4阻害薬*)は不要
- 3. 口腔カンジダ症に対して、抗真菌薬の口腔内投与を行う
- 4. INH予防投与:潜在性結核があり、結核乾癬リスクが高い患者で行われる。生物学的製剤開始3週間前からINHを6ヶ月間投与する
*乾癬に対して保険適用のあるPDE4阻害薬にアプレミラスト(オテズラ®)がある
- 参考:乾癬における生物学的製剤の使用ガイダンス(2019年版) 日皮会誌:129(9), 1845-1864, 2019
関連
- 2020 選択31 (慢性皮膚粘膜カンジダ症を発症する遺伝子異常:IL17F)
選択問題3:解答 1, 2, 3
続発性多汗症の原因疾患を問う問題
- 1. 妊娠:基礎体温の上昇や甲状腺ホルモン増加で、全身性の多汗症をきたし得る
- 2. 糖尿病:甲状腺機能亢進症、低血糖とともに全身性多汗症をきたす代謝異常症。ただし糖尿病で無汗症となることもある→△
- 3. 腋臭症(ワキガ):アポクリン発汗が原因となり、エクリン発汗が原因となる原発性腋窩多汗症を高率に合併する
- 4. コリン性蕁麻疹:特発性後天性全身性無汗症(AIGA)に合併することがある
- 5. アトピー性皮膚炎:汗孔や導管閉塞から無汗症の原因となる(AIGAに合併することもある)
→1, 2, 3では多汗症をきたす
- 参考書籍:あたらしい皮膚科学 第3版 p362-363(1・2・4・5)
- 参考書籍:皮膚科学 第10版 p737-739(1・2・4・5)
- 選択肢3の参考:形成外科診療ガイドラインシリーズ 体幹・四肢疾患 第Ⅱ編 腋臭症 p44
選択肢2の糖尿病について。糖尿病は無汗症の原因ともなり得るため正否の判断が難しいが、他選択肢と比較して相対的に正解選択肢と考えられる
関連問題
- 2021 選択2 / 2012 選択1 (無汗症の原因)
- 2013 選択2 (局所多汗症のうち代償性反応として生じるもの:脳梗塞)
選択問題4:解答 3
角層顆粒細胞内のケラトヒアリン顆粒を構成するプロフィラグリンは、分解されフィラグリン→アミノ酸となり天然保湿因子(natural moisturizing factor)と呼ばれる→3
- 1. 乳酸:グルコースが嫌気性代謝を受けることで産生される
- 2. セラミド:角層細胞間脂質の構成成分の一つで50%を占める。こちらも保湿に重要
- 3. アミノ酸:フィラグリンが分解されるとアミノ酸となり、保水機能や紫外線吸収能を持つ。角層のpHを弱酸性に維持する作用もある
- 4. 分泌型IgA:腸管や唾液などの粘膜で局所免疫に作用し、母乳中にも含まれる
- 5. 低級脂肪酸:アポクリン腺から分泌される汗が細菌で酸化され、低級脂肪酸となり悪臭を引き起こす
アトピー性皮膚炎では、セラミド含有率の低下やフィラグリン発現低下(アトピー性皮膚炎患者の25%にフィラグリンをコードするFLG遺伝子変異がある)により、角質の水分保持能力が低下することが病態に関与している
- 参考書籍:あたらしい皮膚科学 第3版 p9(2・3)/30(4)/361(5)
- 参考書籍:皮膚科学 第10版 p11(3)/13(2)/76(4)/736(5)
関連:2021年度 選択問題10(フィラグリンとその分解産物の作用)
選択問題5:解答 1, 4(現在は4のみ)
男性型脱毛症(AGA)に対する内服薬2種類の違いを問う問題
男性型脱毛症(AGA)と5-α還元酵素阻害薬
男性型脱毛症(AGA)は酵素活性の高いジヒドロテストステロン(DHT)が受容体と結合することが原因となる
治療としてテストステロンからDHTへの変換を行う酵素、5α還元酵素(リダクターゼ)の阻害剤が用いられる
| 作用点 | 一般名 | 商品名 |
| 5-αリダクターゼⅡ型 | フィナステリド | プロペシア® |
| 5-αリダクターゼⅠ型+Ⅱ型 | デュタステリド | ザガーロ® |
いずれも男性ホルモンを低下させるため、性欲減退・勃起機能不全や血清PSA濃度低下が生じる
また男子胎児の生殖器官等の正常発育に影響を及ぼす恐れがあるため、(妊娠している可能性のある)女性への投与は禁忌となっている
- 1. 後発品:現在はいずれも後発品が発売されている(本問出題時はフィナステリドのみ)
- 2. 女性への効果:女性型脱毛症は男性ホルモン依存性でないため無効であり、また上述の利用から投与禁忌(推奨度1D)
- 3. 血清PSA:いずれも低下するため、前立腺癌診断目的では2倍した値を目安として評価する
- 4.5-α還元酵素Ⅰ型:デュタステリドのみが阻害作用を持つ
- 5. 5-α還元酵素Ⅱ型:フィナステリド、デュタステリド双方が阻害作用を持つ
- 参考書籍:あたらしい皮膚科学 第3版 p370-371(3・4・5)
- その他選択肢の参考:男性型および女性型脱毛症診療ガイドライン 2017年版 日皮会誌:127(13), 2763-2777, 2017
関連問題
- 2020 選択88 (5-α還元酵素阻害剤の作用機序)
- 2022 選択21 / 2018 選択4 / 2011 選択4 (男性型脱毛症の治療推奨度)
- 2017 選択6(AGA治療薬の比較)
- 2015 選択5 / 2010 選択3 (フィナステリドについて)
選択問題6:解答 3
尋常性ざ瘡治療ガイドラインにおいて、炎症性皮疹に対しての内服抗菌薬が推奨されている
推奨度が最も高いのはドキシサイクリン(ビブラマイシン®)→3
尋常性痤瘡 炎症性皮疹の内服抗菌薬
| 推奨度 | 一般名 | 製品名 |
| A | ドキシサイクリン | ビブラマイシン® |
| A* | ミノサイクリン | ミノマイシン® |
| B | ロキシスロマイシン | ルリッド® |
| ファロペネム | ファロム® | |
| C1 | テトラサイクリン | アクロマイシン® |
| エリスロマイシン | エリスロシン® | |
| クラリスロマイシン | クラリス® | |
| レボフロキサシン | クラビット® | |
| トスフロキサシン | オゼックス® | |
| シプロフロキサシン | シプロキサン® | |
| ロメフロキサシン | ロメフロン® | |
| セフロキム アキセチル | オラセフ® |
よって本問では
- 1. ファロペネム:B
- 2. ミノサイクリン:A*(めまい・色素沈着等の副作用があるため)
- 3. ドキシサイクリン:A
- 4. クラリスロマイシン:C1
- 5. ロキシスロマイシン:B
ドキシサイクリンは尋常性ざ瘡に対して保険適用がないが、2018年10月に原則として、「ドキシサイクリン塩酸塩水和物【内服薬】」を「ざ瘡(化膿性炎症を伴うもの)」に対して処方した場合、当該使用事例を審査上認める。
と通達が出ており実務上は問題ない
- 参考:尋常性痤瘡治療ガイドライン 2017 日皮会誌:127(6), 1261-1302, 2017のp1273
選択問題7:解答 2, 4
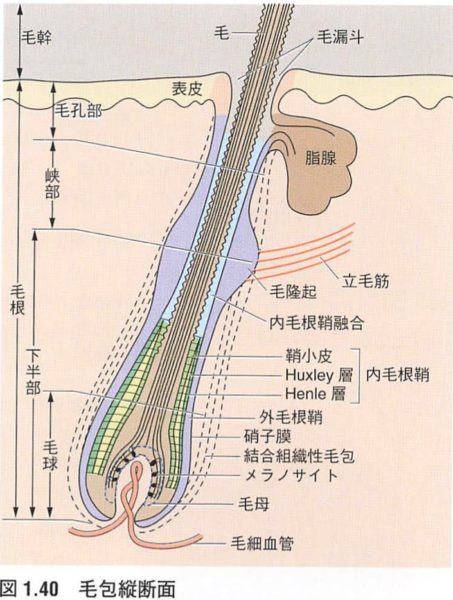
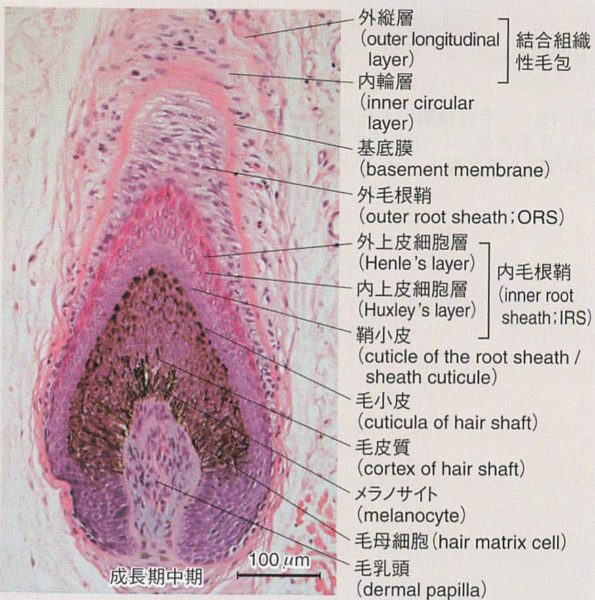
毛包の構造と機能について問う問題
- 1. ①(外毛根鞘):毛包の大部分で最外層に位置するが漏斗部では消失し、被覆表皮が最外層となる。角化する際に顆粒層を介さない特殊な角化形式をとる(外毛根鞘性角化※)
- 2. ②(内毛根鞘):外毛根鞘の内側に位置し、好酸性のトリコヒアリン顆粒を豊富に含有する。ケラトヒアリン顆粒(こちらは好塩基性)に類似
- 3. ③(毛小皮):毛の最外層に位置し、デスモグレイン4を発現する。これをコードするDSG4遺伝子の変異により、常染色体劣性遺伝形式の連珠毛を発症する
- 4. ④(毛乳頭):全ての毛周期で存在するが、休止期には毛母細胞から離れて存在する。血管を含み毛母細胞に栄養を供給する役割を持つ
医療脱毛は毛母に存在するメラニンに反応するレーザーを用いるため成長期の毛には有効だが、毛乳頭と毛母が離れる休止期の毛には有効性が低い
→複数回の照射が必要となる - 5. ⑤(毛母細胞):毛包上皮幹細胞は毛隆起(バルジ領域)に存在する。毛母細胞はメラノサイトを含み、毛にメラニンを供給する
※このため、頭皮に発生し毛包峡部に由来する外毛根鞘性嚢腫では外毛根鞘性角化が特徴となる。一方(外毛根鞘が消失する)漏斗部に由来する粉瘤(表皮嚢腫)は顆粒層を伴う通常の角化形式をとる
- 参考書籍:あたらしい皮膚科学 第3版 p21-23(1・2・4・5) 図1.40/図1.41 引用
- 参考書籍:皮膚科学 第10版 p14-18(1・2・4・5)
- 選択肢3の参考:新・皮膚科セミナリウム 毛髪角化異常症の病態と診断 日皮会誌:126(12), 2269-2274, 2016
関連問題
選択問題8:解答 3
脱毛症に関する一般問題
日本人の先天性乏毛症ではLIPH遺伝子変異の頻度が高い→3
- 1. 抜毛症は自分で毛を抜くことが原因となるため、どの部分でも生じ得る
- 2. 先天性三角形脱毛の病変部では、ダーモスコピーで白色の軟毛が観察される
- 3. 先天性乏毛症は常染色体劣性遺伝形式の疾患で、日本人ではLIPH遺伝子(とくに創始者変異であるc.736T>A)やLPAR6遺伝子変異によるものが多い
- 4. follicular microhemorrhageは抜毛症で抜毛部周囲の毛細血管が破綻して生じる。円形脱毛症では感嘆符毛・漸減毛・黒点がみられる
- 5. 円形脱毛症の場合、ステロイドパルス内服療法はパルス療法後を先に施行して無効の場合に行うため"速やかに移行"することはない
- 参考書籍:あたらしい皮膚科学 第3版 p371(1・3)/370(2)
- 参考書籍:皮膚科学 第10版 p723(1)/720(4)
- 選択肢4の参考:新・皮膚科セミナリウム 毛髪疾患診療のためのトリコスコピーの活用法:病態に基づいたフローチャート法と診断の実際 日皮会誌:131(4), 671-678, 2021
- 選択肢5の参考:日本皮膚科学会 円形脱毛症診療ガイドライン 2017年版 日皮会誌:127(13), 2741-2762, 2017 のp2750
関連問題
- 2023 記述16 / 2016 選択4 (先天性三角形脱毛症)
- 2018 選択5 (円形脱毛症のダーモスコピー)
- 2015 選択3 (乏毛症の原因遺伝子)
選択問題9:解答 4
毛の発生に関する一般問題
毛の発生
胎生9〜12週にまず眉毛・上口唇・オトガイ、続いて顔頭部に毛原基/毛芽が下方に向かって突出してくる
毛芽は皮表に対して斜め45°に伸び、下面から脂腺・アポクリン汗腺・毛隆起が生じる
胎生4〜5ヶ月で全身の毛包発生が終了する
上記より、解答は以下
- 1. 眉毛・上口唇・オトガイが先行するため、頭部は最初ではない
- 2. 脂腺は"下面"から生じる
- 3. 皮表に対して"斜め45°"に伸びる
- 4. 胎生9〜12週間ぐらいで初めて現れる→○
- 5. 胎生"4〜5か月"で全身の毛包の発生が終わる
- 参考書籍:皮膚科学 第10版 p19
選択問題10:解答 1
日本人のスキンタイプ(JST)-IIで健常者にみられる反応を問う問題
UVAとUVBは皮膚で影響を与える部位や日焼けの生じ方が異なる
UVA/UVBの比較と光線過敏症の検査
| 紫外線の種類 | 波長(nm) | 影響部位 | 症状 | 検査 |
| UVA | 320〜400 | 真皮深層まで | サンタン(小麦色の日焼け)
日光弾性線維症(solar elastosis) |
MRD(最小反応量)
健常日本人では10〜15J/cm2 |
| UVB | 290〜320 | 表皮〜真皮浅層 | サンバーン(赤くひりひりする日焼け)
悪性黒子(Lentigo maligna) |
MED*(最小紅斑量)
健常日本人では50〜100mJ/cm2 |
*MED = minimal erythema dose
紫外線に曝露された後の反応は下記のようになる
- 直後:UVAの影響でもともと持っているメラニンが黒くなる反応(即時型黒化)が起こる
- 4時間後〜:UVBの影響によるサンバーンが起こり、24時間後をピークとして3日程度で消退
- 10時間後〜:メラニン合成が促進し、サンタンが生じる。照射量によっては数カ月間持続する
上記より解答は以下となる
- 1. 20J/cm2でも即時型黒化は生じるため、健常人でも見られる反応→○
- 2. 健常人では通常UVA照射による紅斑は生じず、サンタンのみ
- 3・4. 20mJ/cm2のUVBは健常人のMED以下であるため、反応は生じない。またUVBは即時型黒化をきたさない
- 5. スライドプロジェクター:可視光線の光線過敏を検査するもので、15〜20分照射して反応がでれば過敏(慢性光線性皮膚炎や日光蕁麻疹で陽性)
- 参考書籍:あたらしい皮膚科学 第3版 p84/228/230
- 参考書籍:皮膚科学 第10版 p110/263
- 参考:新・皮膚科セミナリウム 光線過敏症診断のための検査法 日皮会誌:133(10), 2325-2336, 2023
- 参考書籍:皮膚科臨床アセット シミと白斑 最新診療ガイド p148-151
- 参考:皮膚科セミナリウム 第58回 光線(赤外線・可視光線・紫外線)による皮膚障害 日皮会誌:120(2), 201―206, 2010
- 参考:新・皮膚科セミナリウム 病院における光線過敏症患者への対応 日皮会誌:127(13), 2785-2789, 2017
関連問題
- 2016 記述1 (UVAによる即時型黒化)
- 2013 選択6 (即時型黒化をもたらす紫外線波長)
- 2012 選択4 (即時黒化の臨床問題)
選択問題11:解答 3, 4
紫外線に関する一般問題
UVAとUVBの比較については上記選択問題10を参照
- 1. 波長が400nm"以下"(190nm以上)のものを紫外線と呼ぶ
- 2. 波長が"短い"方から、UVC<UVB<UVAの順番となる。V=fλであり、波長が短いほど振動数が高くエネルギーが高い
- 3・5. UVAはUVBよりも透過性が高いため、通常の窓ガラスを通過し真皮でコラーゲンやエラスチンにダメージを与える(solar elastosisの原因となる)
- 4. 外因性光線過敏症の原因となるのは主にUVA。内因性光線過敏症の一つ慢性光線性皮膚炎ではUVBに対するMEDが低下する
- 参考書籍:あたらしい皮膚科学 第3版 p107(1・2)/229(4)
- 参考書籍:皮膚科学 第10版 p263〜265
関連問題
- 2023 選択57 (薬剤性光線過敏症の原因波長)
- 2021 選択9 (UVAが引き起こす疾患)
- 2022 選択31 / 2014 選択3 / 2013 選択6 (UVA/UVBについて)
- 2020 選択5 (紫外線の波長の単位)
選択問題12:解答 5
顔面から頚部にかけて雀卵斑様の色素斑が多発しており、50歳と比較的若年から基底細胞癌が多発している
神経学的異常がないことから、光線過敏症の中でも色素性乾皮症 V型を疑う
V型では不定期DNA合成能(UDS)は正常値となる→5
色素性乾皮症(XP)
常染色体劣性遺伝疾患で、紫外線によるDNA損傷を修復する機構に異常があり若年から皮膚悪性腫瘍を合併しやすい
原因遺伝子によってA〜G群+V型に分けられ、A〜G群ではDNA除去修復酵素に異常が、V型は損傷乗り越え複製機構に異常がある
C群/E群/V型には神経症状がない・サンタン型(色素異常型)・MED低下がないなどの共通項がある
- 1・2. CS遺伝子変異が原因となるのはコケイン症候群で、光線過敏症の他早老症や難聴を合併するが高発癌性ではない※。XP-V型の原因遺伝はPOLHで、確定診断に有用
- 3.紫外線感受性試験:XP-V型は正常〜軽度高感受性にとどまり、V型以外は高感受性
- 4. RNA合成回復能(RRS):コケイン症候群ではRRSが低下する
- 5. UDS:V型の病因はDNA損傷乗り越え複製(複製の際に損傷があっても、それを乗り越えて複製を行う機構)の異常であり、UDSは正常値。V型以外は低下する
※ただしコケイン症候群に色素性乾皮症を合併する場合があり、この場合当然高発癌性となる
- 参考書籍:あたらしい皮膚科学 第3版 p234-236(1・2・5)
- 参考書籍:皮膚科学 第10版 p274(1)/271(2・3・5)
- 選択肢4の参考:コケイン症候群(指定難病192) – 難病情報センター
本問で与えられた臨床情報からは、XP-V以外にXP-EやXP-F(比較的高齢になってからの発癌かつ神経症状に乏しい)の可能性を厳密には否定できない。またXP-EやFの紫外線感受性試験は「きわめて低い」というほど低値をとらない。この場合、選択肢3が正解で選択肢5が誤りとなる。
作成者は疫学的な問題(XP-Vは日本人XP患者の25%を占める)からXP-Vと想定し、選択肢5を想定正答とした。
関連問題
- 2020 選択6 / 2015 選択6 (XPについて:頻度・検査結果・神経症状の有無など)
- 2018 選択7 (XP-Vについて)
- 2013 選択5 (若年から発癌をきたしやすい病型)
- 2010 選択6 (XP-Vについて)
選択問題13:解答 5
メラニン合成に関する問題
メラノサイト内に存在する細胞内小器官、メラノソームで合成される→5
- 1. メラニンは"チロシン"から合成される
- 2. メラノサイト内の”メラノソーム内”で合成され、ケラチノサイト(角化細胞)に供給される
- 3. 律速酵素はチロシナーゼであり、同部位の遺伝子変異でOCA*1型を発症する。DHICA oxidase活性を有するのはTYRP1で、OCA3型の原因となる
- 4. 多くの日本人はユーメラニン(黒色)優位である。フェオメラニン(黄色)優位では赤毛となる
- 5. メラノサイト内の脂質二重膜で囲まれた細胞内小器官、メラノソームで合成される。このメラノソームの膜表面に発現する遺伝子がMATPであり、同遺伝子変異はOCA4型の原因となる
*OCA = 眼皮膚白皮症
- 参考書籍:あたらしい皮膚科学 第3版 p10-11(ALL)/304(3)/23(4)
- 参考書籍:皮膚科学 第10版 p29-31(1・2・4)/517(3)/18(4)
関連問題
選択問題14:解答 3, 4
ケラチンの発現部位を問う問題
掌蹠で発現するタイプIケラチンはケラチン9/17がある→3, 4
ケラチンと先天性皮膚疾患
ケラチンは角化細胞の細胞骨格を担い、酸性のタイプⅠケラチンと中性〜塩基性のタイプⅡケラチンが重合して中間経線維を形成する
- タイプⅠケラチン:ケラチン9〜40
- タイプⅡケラチン:ケラチン1〜8
組織によって発現するケラチンが異なり、またケラチン関連の遺伝子変異により先天性皮膚疾患を合併する
| ケラチン | 発現組織 | 疾患 |
| 1/10 | 有棘細胞 | 表皮融解性魚鱗癬 (水疱型先天性魚鱗癬様紅皮症) |
| 1/9 | 有棘細胞(掌蹠) | Vörner 型掌蹠角化症 |
| 2/10 | 有棘層上層〜顆粒層 | 表在性表皮融解性魚鱗癬 (Siemens型水疱性魚鱗癬) |
| 3/12 | 角膜上皮細胞 | Meesmann角膜ジストロフィ |
| 4/13 | 粘膜上皮 | 白色海綿状母斑 |
| 5/14 | 基底細胞 | 単純型表皮水疱症 |
| 6a・6b/16・17 | 爪 | 先天性爪甲肥厚症 |
掌蹠角化症を引き起こす中で、タイプⅠケラチンに該当するのはケラチン9と17となる
-

-
ケラチン 発現部位と先天性皮膚疾患 まとめ
続きを見る
- 1. ケラチン1:掌蹠有棘細胞で発現するが、タイプIIケラチン
- 2. ケラチン5:基底細胞で発現するタイプIIケラチン
- 3. ケラチン9:掌蹠有棘細胞で発現するタイプIケラチン
- 4. ケラチン17:爪で発現するタイプIケラチン。先天性爪甲肥厚症が掌蹠角化症を伴うことからわかるように、掌蹠にも発現する
- 5. ケラチン25:毛包内毛根鞘で発現するタイプIケラチンで、常染色体劣性縮毛症の原因となる
- 参考書籍:あたらしい皮膚科学 第3版 p8
- 参考書籍:皮膚科学 第10版 p11
- 選択肢5の参考:毛髪角化異常症の病態と診断 日皮会誌:126(12), 2269-2274, 2016 のp2269
関連:ケラチンの発現部位を問う問題は頻出。上記記事にまとめた
選択問題15:解答 2
Cornified cell envelope(周辺帯)の主成分を問う問題
インボルクリンやロリクリンから構成され、角層細胞の外側に存在する →2
- 周辺帯:角層の細胞膜を裏打ちする構造物で、インボルクリンやロリクリンなどの蛋白がトランスグルタミナーゼにより架橋することで作られる※
- filaggrin(フィラグリン):顆粒細胞のケラトヒアリン顆粒に存在するプロフィラグリンが分解を受けて産生される。さらに分解を受けることで天然保湿因子(NMF)となり、保水や紫外線吸収に働く
- keratin(ケラチン):細胞内骨格を構成するタンパクで、種類により発現部位が異なる。フィラグリンとケラチンでケラチン模様を形成し、角層細胞の内側を構成する
※ロリクリンの変異でロリクリン角皮症、トランスグルタミナーゼの変異で葉状魚鱗癬と角化異常症を発症する
- 参考書籍:あたらしい皮膚科学 第3版 p8-9/274
- 参考書籍:皮膚科学 第10版 p11-12
関連
- 2017 選択11 (角層細胞から細胞間脂質への並び順)
- 2016 選択9 / 2013 選択11 / 2011 選択8 (周辺帯の構成成分)
選択問題16:解答 3
ケラチンは3つのドメイン(ヘッドドメイン・ロッドドメイン・テイルドメイン)から構成される
ケラチン異常症は重合に関わるロッドドメインの両端(1Aおよび2B)領域に多い→3
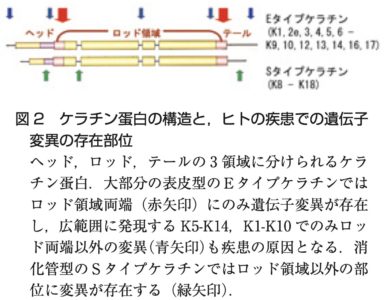
参考文献より引用
- 参考書籍:皮膚科学 第10版 p11
- 図引用・参考:皮膚科セミナリウム 第23回 ケラチン 日皮会誌:117(2), 129-135, 2007
選択問題17:解答 1, 3, 4
アトピー性皮膚炎の痒みへ直接関与すると考えられているサイトカインは、IL-4/13/31の3つ→1, 3, 4
生物学的製剤のターゲットとなっている
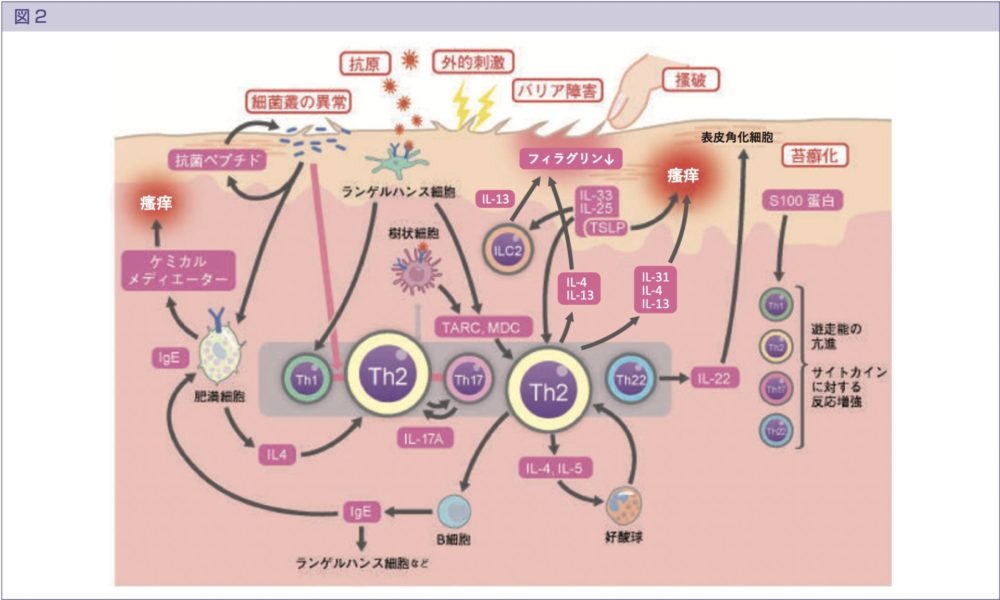
参考文献より引用
下記も参照
-

-
アトピー性皮膚炎 サイトカインと生物学的製剤、JAK阻害薬について
続きを見る
- 1. IL-4:Th2細胞から分泌され、角化細胞でのフィラグリン発現低下や掻痒、好酸球遊走に関与する。デュピルマブ(デュピクセント®)のターゲット
- 2. IL-5:Th2細胞から分泌され、好酸球遊走に関与する。同部位をターゲットとするメポリズマブ(ヌーカラ®)は好酸球を減少させるが、アトピー性皮膚炎での皮疹や掻痒に対する効果は証明されていない
- 3. IL-13:Th2細胞から分泌され、角化細胞でのフィラグリン発現低下や掻痒に関与する。デュピルマブおよびトラロキヌマブ(アドトラーザ®)のターゲット
- 4. IL-31:Th2細胞から分泌され、掻痒に関与する。同部位をターゲットとするネモリズマブ(ミチーガ®)が最近アトピー性皮膚炎に対して承認された
- 5. IL-36:角化細胞から分泌され、汎発性膿疱性乾癬や炎症性腸疾患の病態に関与する。同部位をターゲットとするスペビゴ®が2022年11月に発売となった※
※スペビゴ®(スペソリマブ)の保険適用は「膿疱性乾癬における急性症状の改善」
- 参考書籍:あたらしい皮膚科学 第3版 p287(5)
- 参考・図引用:アトピー性皮膚炎診療ガイドライン 2021 日皮会誌:131(13), 2691-2777, 2021
- IL-5の参考:アトピー性皮膚炎の発症機序; AHR軸とIL-13/IL-4-JAK-STA6/STAT3軸による競合的皮膚バリア調節機構 日皮会誌:130(13), 2705-2723, 2020
関連問題
アトピー性皮膚炎に関わるサイトカインについての出題は近年頻出。上記記事にもまとめた
選択問題18:解答 3, 4, 5
T細胞の機能抑制に関与するのはCTLA-4, PD-1, IDOがある→3, 4, 5
腫瘍免疫は抗原提示細胞による"誘導相"とT細胞が反応する"効果相"に分けられる
主に前者で働くのがCTLA-4、後者で働くのがPD-1
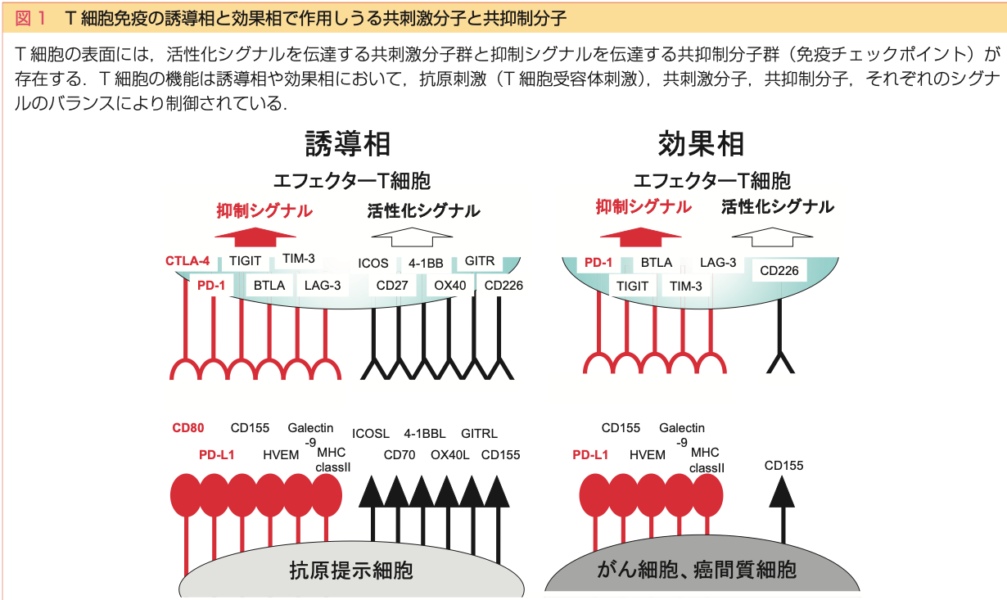
参考文献より引用
メラノーマなど悪性腫瘍では、T細胞の機能抑制を利用し腫瘍免疫から逃避する機構が存在する
この「抑制を解除」し、腫瘍免疫を賦活化させることを目的とした薬剤が免疫チェックポイント阻害剤として利用されている
- 1・2. CD134(OX40)・CD137(4-1BB):活性化シグナルとして作用する
- 3. CD152(CTLA-4):同部位に作用する薬剤にイピリムマブ(ヤーボイ®)がある
- 4. CD279(PD-1):同部位に作用する薬剤にニボルマブ(オプジーボ®)やペムブロリズマブ(キイトルーダ®)がある
- 5. IDO:トリプトファン代謝に関わる。悪性腫瘍で高発現となり、リンパ球の作用に必要なトリプトファンを枯渇させる
同部位に作用する薬剤にエパカドスタットがある(悪性黒色腫で治験を行っていたが有効性が証明できず終了となった)
なお上記図に含まれる中だと、抗LAG3抗体relatlimabが米国で悪性黒色腫に対して承認され、第3の免疫チェックポイント阻害剤となった
- 参考および図引用:新・皮膚科セミナリウム 免疫チェックポイント阻害剤の効果と副作用 日皮会誌:128(6), 1291-1299, 2018
- 選択肢5の参考:免疫代謝とがん免疫治療 医学のあゆみ Vol. 271 No.2, 2019
関連問題
- 2020 記述19 / 2016 記述9 (イピリムマブのターゲット分子)
- 2016 選択79 (T細胞の活性化を抑制する分子)
選択問題19:解答 1, 2
アレルゲンコンポーネント特異的IgE検査と原因タンパクを問う問題
アレルゲンコンポーネント検査
従来のアレルギー検査では「大豆」「牛乳」などの蛋白質(粗抗原)に対するIgEを測定していた
ただ粗抗原には複数のアレルゲンコンポーネントが含まれるため、アレルゲンコンポーネント特異的IgE検査を施行することでより感度・特異度の高い検査が可能となる
下記10種類のアレルゲンコンポーネントが保険適用となっている
| 由来 | コンポーネント名 | 蛋白名 |
| 卵白 | Gal d 1 | オボムコイド |
| 牛乳 | Bos d 4 | αラクトアルブミン |
| Bos d 5 | βラクトグロブリン | |
| Bos d 8 | カゼイン | |
| 小麦 | Tri a 19 | ω-5グリアジン |
| 大豆 | Gly m 4 | PR-10 |
| ピーナッツ | Ara h 2 | 2Sアルブミン |
| クルミ | Jug r 1 | |
| カシューナッツ | Ana o 3 | |
| ラテックス | Hev b 6.02 | ヘベイン |
よって、本問の解答は下記となる
- 1. 卵白:Gal d 1 (オボムコイド)→○
- 2. 牛乳:Bos d 8 (カゼイン)→○
- 3. 大豆:Gly m 4 (PR-10)→✗、Ara h 2はピーナッツ
- 4. ピーナッツ:Ara h 2 (2Sアルブミン)→✗、Bet v 1はシラカンバ ※口腔アレルギー症候群の原因となり、Gly m 4と高い相同性を有する
- 5. ラテックス:Hev b 6.02 (ヘベイン)→✗、Gly m 4は大豆
関連問題
- 2022 選択32 / 2021 選択67 (アレルゲンコンポーネントについて)
- 2020 選択52 / 2019 選択64 / 2018 記述6 (PR-10によるPFASと原因樹木・コンポーネント)
- 2016 選択53(食物とアレルゲン)
選択問題20:解答 1
図4aでは前頚部露光部で紅色〜褐色斑が多発している
図4bでは組織学的に明るい細胞質がみられ、ヒトパピローマウイルスによる感染が示唆される
いとこ婚で遺伝性疾患のリスクが高く、幼少期から上記皮疹を認めることから疣贅状表皮発育異常症の診断
疣贅状表皮発育異常症
常染色体劣性遺伝疾患で、TMC6やTMC8遺伝子の異常が原因となる
先天的にHPV(human papillomavirus)に対する免疫異常があり、全身とくに露光部で扁平疣贅様の疣贅状病変が多発(HPV-5/8/17/20などが原因)し、青年期に有棘細胞癌など悪性腫瘍へ進展する
癜風に類似した所見となることもある
組織学的には細胞質が明るく腫大した澄明変性細胞が有棘層上層〜顆粒層でみられる
- 1. Beta human papillomavirus:疣贅状表皮発育異常症の原因→○
- 2. Candida albicans:指間びらん症や間擦疹、慢性皮膚粘膜カンジダ症等の原因
- 3. Cytomegalovirus(サイトメガロウイルス):皮膚科領域では伝染性単核球症(の一部)やGianotti-Crosti症候群の原因
- 4. Epstein-Barr virus(EBウイルス):伝染性単核球症の原因で、慢性化すると慢性活動性EBウイルス感染症となる
- 5. Malassezia globosa(マラセチア):癜風やマラセチア毛包炎の原因で、脂漏性皮膚炎やアトピー性皮膚炎との関与も指摘される
- 参考書籍:あたらしい皮膚科学 第3版 p497(1)/537(2)/505・507(3・4)/540(5)
- 参考書籍:皮膚科学 第10版 p774(1)/865(2)/765(3)/763(4)/872(5)
関連問題
- 2020 選択28 (疣贅状表皮発育異常症の原因HPV)
選択問題21:解答 4, 5
アトピー性皮膚炎の病態に関わるサイトカインの多くはTh2細胞から分泌され、掻痒感やフィラグリン発現低下に関与する
一方バリア機能が障害されるとケラチノサイトから分泌されるサイトカイン(IL-33やTSLP)は、Th1/Th2バランスをTh2優位にする作用がある→4, 5
これによって、Th2細胞優位
→Th2細胞から分泌されるサイトカインが掻痒・掻爬を引き起こす
→皮膚バリアがさらに悪化
という負のスパイラルへ陥る
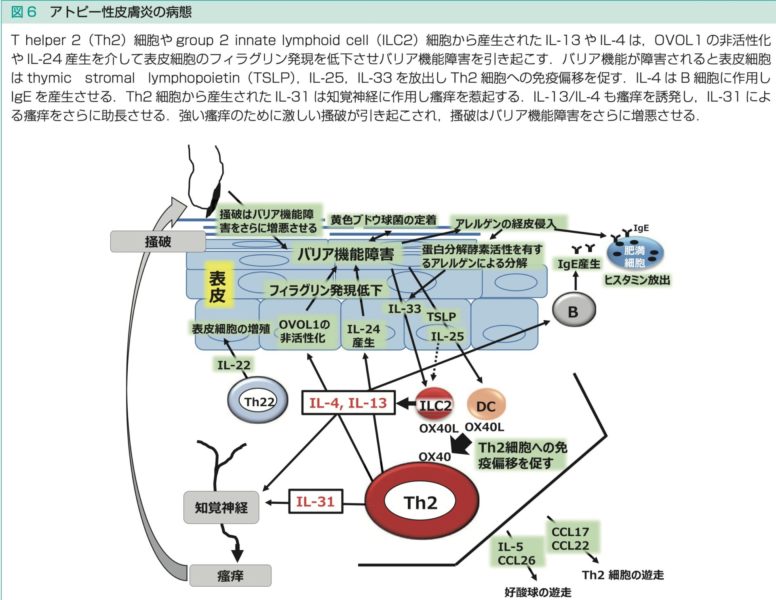
参考文献より引用
アトピー性皮膚炎とサイトカインについては下記も参照
-

-
アトピー性皮膚炎 サイトカインと生物学的製剤、JAK阻害薬について
続きを見る
- 1. IL-4:Th2細胞から分泌され、角化細胞でのフィラグリン発現低下や掻痒、好酸球遊走に関与する。デュピルマブ(デュピクセント®)のターゲット
- 2. IL-5:Th2細胞から分泌され、好酸球遊走に関与する。同部位をターゲットとするメポリズマブ(ヌーカラ®)は好酸球を減少させるが、アトピー性皮膚炎での皮疹や掻痒に対する効果は証明されていない
- 3. IL-13:Th2細胞から分泌され、角化細胞でのフィラグリン発現低下や掻痒に関与する。デュピルマブおよびトラロキヌマブ(アドトラーザ®)のターゲット
- 4. IL-33:ケラチノサイトから分泌され、Th2型優位への免疫偏移を引き起こす。同部位をターゲットとするイテペキマブは喘息において有効とされ、皮疹の改善も報告されている
- 5. TSLP:ケラチノサイトから分泌され、Th2型優位への免疫偏移を引き起こす。同部位をターゲットとするテゼペルマブは喘息治療薬として米国で承認されているが、アトピー性皮膚炎においては臨床効果が得られなかった
- 図引用・参考:アトピー性皮膚炎の発症機序; AHR軸とIL-13/IL-4-JAK-STA6/STAT3軸による競合的皮膚バリア調節機構 日皮会誌:130(13), 2705-2723, 2020
関連問題
Th2細胞が分泌するサイトカインに関する問題もあり、上記カード参照
選択問題22:解答 4
自己炎症症候群や遺伝性皮膚疾患の原因遺伝子を問う問題
本問の3疾患はまとめてクリオピリン関連周期熱症候群と呼ばれ、NLRP3が病原遺伝子→4
クリオピリン関連周期熱症候群
炎症の初期反応を制御するクリオピリン(NLRP3遺伝子:別名CIAS1遺伝子)の変異によりNF-κBが活性化→IL-1βが過剰産生され、寒冷刺激による膨疹や関節痛・発熱発作をきたす
臨床症状の程度により、3つに分類される
- 家族性寒冷蕁麻疹(軽症)
- Muckle-Wells症候群(中等症)
- 慢性乳児神経皮膚関節炎症候群:CINCA症候群(重症)
治療薬としてIL-1βをターゲットとするカナキヌマブ(イラリス®)やアナキンラ(日本未承認)がある
- 1. IL36RN:汎発性膿疱性乾癬、とくに尋常性乾癬の先行しない病型の原因遺伝子※
- 2. LPAR6:常染色体劣性遺伝形式の先天性乏毛症の原因遺伝子の一つ(日本人で最多はLIPH)
- 3. NF1:神経線維腫症1型の原因遺伝子で、遺伝子産物はニューロフィブロミン
- 4. NLRP3:クリオピリン関連周期熱症候群の原因遺伝子
- 5. NOD2:Blau症候群の原因遺伝子。乳幼児に肉芽腫を生じ、若年性サルコイドーシスとも呼ばれる疾患
※IL36受容体阻害因子欠損症はDITRAと呼ばれ、汎発性膿疱性乾癬がその代表疾患
- 参考書籍:あたらしい皮膚科学 第3版 p217-218(4・5)/287(1)/391(3)
- 参考書籍:皮膚科学 第10版 p170(4)/379(1)/544(3)
- 選択肢2の参考:新・皮膚科セミナリウム 毛髪角化異常症の病態と診断 日皮会誌:126(12), 2269-2274, 2016
関連問題
選択問題23:解答 2
常染色体半優性遺伝疾患では、遺伝子変異をhetero接合体で保有している場合でも症状を発症するが、homo接合体や複合ヘテロ接合体で保有している場合重症型を示す
フィラグリンをコードするFLG遺伝子変異による尋常性魚鱗癬が代表例→2
- 1. 葉状魚鱗癬:周辺帯形成に関与するTGM1遺伝子変異により発症し、常染色体劣性遺伝形式をとる
- 2. 尋常性魚鱗癬:FLG遺伝子変異をhomo接合体ないし複合hetero接合体で保有する場合、臨床像が重症となる
- 3. 道化師様魚鱗癬:層板顆粒からの角質細胞間脂質の分泌に関わるABCA12遺伝子変異(nonsense変異)により発症し、常染色体劣性遺伝形式をとる
- 4. 表皮融解性魚鱗癬:細胞骨格をコードするKRT1/10遺伝子変異により発症し、常染色体優性遺伝形式をとる。組織学的に顆粒変性を伴うことが特徴
- 5. 先天性魚鱗癬様紅皮症:ABCA12遺伝子変異(missense変異)やTGM1遺伝子変異によって発症し、常染色体劣性遺伝形式をとる。ゴミ箱的病名であり、複数の原因遺伝子が存在する
ケラチンは複数が重合(32量体)して中間経フィラメントとして機能するため、1つに変異があるだけで症状をきたすようになる
→ケラチンが原因の魚鱗癬・掌蹠角化症は常染色体優性遺伝形式(ここでは表皮融解性魚鱗癬)
- 参考書籍:あたらしい皮膚科学 第3版 p269(2)/271(1・3・5)/273(4)
- 参考書籍:皮膚科学 第10版 p329(2)/334(1・5)/335(3)/332(4)
選択問題24:解答 1
層板顆粒に存在する脂質輸送タンパクをコードし、角層細胞間脂質の分泌に関与する遺伝子はABCA12→1
同遺伝子の変異で、道化師様魚鱗癬を発症する。最重症の魚鱗癬で、眼瞼外反・口唇突出など特徴的な所見を呈する
その他選択肢については下記参照
魚鱗癬の原因遺伝子
| 原因遺伝子 | 遺伝形式 | |
| 尋常性魚鱗癬 | FLG | 常染色体半優性遺伝 |
| X連鎖性魚鱗癬 | STS | X連鎖劣性 |
| 道化師様魚鱗癬 | ABCA12 | 常染色体劣性 |
| 葉状魚鱗癬 | TGM1等 | 常染色体劣性 |
| 先天性魚鱗癬様紅皮症 | ABCA12, TGM1等複数 (ゴミ箱的診断) |
常染色体劣性 |
| 表皮融解性魚鱗癬 | KRT1/KRT10 | 常染色体優性 |
| 表在性表皮融解性魚鱗癬 | KRT2e | 常染色体優性 |
※ケラチン症性魚鱗癬は、dominant negative効果のため常染色体優性遺伝形式をとる
- 参考書籍:あたらしい皮膚科学 第3版 p271(1・5)/268(2)/273(3)/270(4)
- 参考書籍:皮膚科学 第10版 p335(1)/329(2)/332(3)/331(4)/334(5)
関連問題
- 2022 選択5 (道化師様魚鱗癬の症状・原因遺伝子・治療など)
- 2021 記述1(皮膚の保湿に関連する因子)
- 2016 選択12(臨床写真があるがほぼ同一問題)
選択問題25:解答 5
図5a, bでは掌蹠のびまん性過角化および一部アキレス腱での潮紅を伴う皮疹(掌蹠を越える皮疹:transgrediens)がみられる
水暴露で浸軟するという特徴的な所見と合わせて、長島型掌蹠角化症の診断
長島型掌蹠角化症
日本含むアジアで最も高頻度に見られる掌蹠角化症で、セリンプロテアーゼインヒビターの一種SERPINB7遺伝子変異による常染色体劣性遺伝疾患
とくにc.796 C>T(p.Arg266*)が創始者変異で、保有率が高い
症状としては肘頭部やアキレス腱部など、掌蹠を越える部位で潮紅を伴う皮疹がみられるtransgrediensや短時間の浸水で患部が浸軟することが特徴。掌蹠多汗による悪臭や白癬の合併が多い
- 1. SERPINB7遺伝子変異による、常染色体劣性遺伝疾患。ただし保有率が2%と高く、一見常染色体優性遺伝形式のように見える(偽優性遺伝形式)ことがある
- 2. 病変部では多汗や悪臭を認め、足白癬の合併が多い
- 3. 組織学的には顆粒層直上(角層最下層)に数層の不全角化がみられる
- 4. 病原性変異の多くはc.796C>Tであり、ナンセンス変異に該当する※
- 5. SERPINB7は顔面や腹部でも発現がみられ、全身の皮膚に存在する→ので掌蹠以外でも症状があると思われる
(なぜ掌蹠優位に病変が見られるかはわかっていない)
※ナンセンス変異:終止コドンによりタンパク合成が途中で終了するタイプの変異↔ミスセンス変異:アミノ酸置換を生じる変異
一般にナンセンス変異の方が合成されるタンパク質に与える影響が大きいため、重篤な症状をきたしやすい(ex. ABCA12遺伝子変異はナンセンス変異であると道化師様魚鱗癬の、ミスセンス変異であると葉状魚鱗癬の原因となり前者の方が重篤)
- 参考書籍:あたらしい皮膚科学 第3版 p277(1・2)
- 選択肢3の参考:掌蹠角化症診療の手引き 日皮会誌:130(9), 2017-2029, 2020のp2019
- 選択肢4の参考:長島型掌蹠角化症-疾患の発見から原因遺伝子の解明へ- 久保 亮治(皮膚科)|KOMPAS
- 選択肢5の参考:Mutations in SERPINB7, encoding a member of the serine protease inhibitor superfamily, cause Nagashima-type palmoplantar keratosis Am J Hum Genet. 2013 Nov 7;93(5):945-56. のp951-952(Fig.3D)
関連問題
- 2022 選択77 / 2015 選択14 (原因遺伝子, 症状)
- 2021 選択91(セリンプロテアーゼインヒビターの変異で発症する疾患)
- 2020 選択14 (浸水試験, 皮疹部位, 偽優性遺伝形式)
選択問題26:解答 5
角化症の一つ、固定性扁豆(へんず)状角化症に関する一般問題
固定性扁豆状角化症 (heperkeratosis lenticularis perstans)
中高年の両側四肢(足背や手背)に好発し、直径1〜5mmの赤色〜褐色調角化性丘疹がみられる。角質部をはがすと点状出血をきたす
家族内発症があり常染色体優性遺伝と考えられているが、原因不明
組織学的には角質が肥厚し、表皮や顆粒層の菲薄化/消失する。表皮真皮境界部での単核球浸潤(苔癬様変化)もみられる
治療ではエトレチナート内服やビタミンD外用が用いられる
- 参考書籍:あたらしい皮膚科学 第3版 p300(1・2・4)
- 参考書籍:皮膚科学 第10版 p349(1〜4)
- 選択肢5の参考:家族内発症を伴う固定性扁豆状角化症の1例 皮膚科の臨床 59巻4号 p431-434, 2017
選択問題27:解答 4
毛孔性紅色粃糠疹に関する一般問題
古典的成人発症型(Griffiths I型)は自然治癒率が高い→4
毛孔性紅色粃糠疹(PRP:pityriasis rubra pilaris)の病型分類
四肢伸側で毛孔一致性の角化性丘疹をきたす疾患で、組織学的には不全角化と正常角化が交互配列することが特徴
古典的にはⅠ〜Ⅴ型に分類されるが、HIV感染と関連した型(Ⅵ型)も存在する
| Griffiths分類 | 発生率(%) | 3年以内寛解率 | 特徴 |
| Ⅰ型(成人古典型) | 55 | 81 | 急性発症 |
| Ⅱ型(成人非典型型) | 5 | 20 | 魚鱗癬様で慢性経過 |
| Ⅲ型(小児古典型) | 10 | 16 | 2歳以前に発症 |
| Ⅳ型(小児限局型) | 25 | 32 | 肘膝で毛孔性角化、進展しない |
| Ⅴ型(小児非典型型) | 5 | 0 | CARD14遺伝子と関連し、早期発症で慢性経過 |
| Ⅵ型(HIV関連型) |
※皮膚科学 第10版 p380 表16-3に追記
CARD14遺伝子の変異/多型はPRPⅤ型と関連し、家族性乾癬や膿疱性乾癬も発症することがある
- 1. HIVと関連した病型が存在し、Ⅵ型に分類される
- 2. 活性型ビタミンD3外用薬のうち、タカシトール(ボンアルファ®)のみPRPに保険適用がある
- 3. 抗IL-12/23 p40抗体製剤(ウステキヌマブ:ステラーラ®)や抗TNF-α抗体製剤が有効であった例が報告されている(保険適用外)
- 4. 成人は2〜3年、若年は1年で自然治癒する。CARD14遺伝子と関連するⅤ型(小児非典型型)は小児発症で慢性経過をとり自然治癒しない
- 5. 思春期前後の小児発症型(Ⅳ型)は肘や膝の角化性丘疹が特徴
- 参考書籍:あたらしい皮膚科学 第3版 p288-289(1・2・4)
- 参考書籍:皮膚科学 第10版 p380-382(1・2・4・5)
- 選択肢3の参考:毛孔性紅色粃糠疹の遺伝学的背景 臨床皮膚科 最近のトピックス2018 72巻5号 p55-59, 2018
関連問題
- 2021 選択23(PRPの臨床問題)
- 2020 選択18 (膿疱性乾癬の原因遺伝子)
- 2020 選択17 / 2010 選択12 (PRPの病理)
選択問題28:1, 2, 3
アプレミラスト(オテズラ®)に関する問題
- 1. 妊婦又は妊娠している可能性のある女性にはアプレミラストやメトトレキサートは投与禁忌。シクロスポリン(ネオーラル®)は妊婦も投与可能
- 2. 紫外線療法:アプレミラストは併用可能。シクロスポリンは皮膚癌の発現を促進する可能性があり、併用注意
- 3. cAMPに特異的なホスホジエステラーゼ(PDE)4を阻害することで、細胞内cAMP濃度を上昇させIL-17やTNF-αなど炎症性サイトカインの分泌を抑制する
- 4. 適応疾患は尋常性乾癬(局所療法で効果不十分)および"関節症性"乾癬で膿疱性乾癬は適応外。ベーチェット病による口腔潰瘍にも適用がある
- 5. 開始時は下痢や頭痛の副作用を軽減するため、"6日間"かけて常用量(30mg 2錠)まで増量する
関連問題
選択問題29:解答 2
抗TNF-α抗体製剤の投与により、多発性硬化症等の脱髄疾患を再燃/悪化させる恐れがある
そのため尋常性乾癬で用いられるTNFα抗体製剤はいずれも、添付文書上投与禁忌となっている→2
- 1. IL-17阻害剤:真菌感染症(とくにカンジダ症)の副作用があり、炎症性腸疾患にも注意が必要
- 2. TNFα阻害剤:脱髄性疾患やループス様症候群(抗核抗体や抗dsDNA抗体陽性化)、うっ血性心不全が特有の注意点
- 3. IL-23 p19阻害剤:特有の注意点はない
- 4. エトレチナート(チガソン®):催奇形性が強いため妊娠は禁忌(服薬終了後2年間は避妊)。肝機能障害・脂質異常症に注意が必要
- 5. シクロスポリン(ネオーラル®):CYP3A4を阻害するロスバスタチン等との併用禁忌。腎障害や高血圧に注意が必要
※結核や重篤な感染症への注意は生物学的製剤全般で共通
乾癬 生物学的製剤の一般名と商品名
| 標的分子 | 商品名 | 一般名 |
| TNF-α | レミケード® | インフリキシマブ |
| ヒュミラ® | アダリムマブ | |
| シムジア® | セルトリズマブ ペゴル | |
| IL-17 | コセンティクス® | セクキヌマブ |
| トルツ® | イキセキズマブ | |
| ルミセフ® | ブロダルマブ | |
| ビンゼレックス® | ビメキズマブ | |
| IL-23 p19 | トレムフィア® | グセルクマブ |
| スキリージ® | リサンキズマブ | |
| イルミア® | チルドラキズマブ | |
| IL-12/23 p40 | ステラーラ® | ウステキヌマブ |
- 参考:乾癬における生物学的製剤の使用ガイダンス (2019年版) 日皮会誌:129(9), 1845-1864, 2019
関連問題(乾癬の生物学的製剤)
- 2023 選択43 (★同一問題★)
- 2017 選択20 (IL-17A関連薬剤の投与スケジュール)
- 2014 選択15 (レミケード®の投与量)
- 2013 選択20 (乾癬治療の標的分子:TNF-α, IL-12/23p40, IL-17)
- 2012 選択14 / 2011 選択14 (TNF-α阻害薬投与時の注意)
選択問題30:解答 3, 4
抗ヒスタミン薬の添付文書における投与可能年齢を問う問題
6ヶ月から投与可能な抗ヒスタミン薬はザイザル®・ザジテン®・アレグラ®の3種類
→3・4
抗ヒスタミン薬(抗アレルギー薬) 投与可能年齢
| 年齢 | 一般名 | 商品名 |
| 6ヶ月〜 | ケトチフェン | ザジテン® |
| フェキソフェナジン | アレグラ® | |
| レボセチリジン | ザイザル® | |
| 1歳〜 | メキタジン | ニポラジン®
ゼスラン® |
| 2歳〜 | オロパタジン | アレロック® |
| セチリジン | ジルテック® | |
| 3歳〜 | エピナスチン | アレジオン® |
| ロラタジン | クラリチン® | |
| 7歳〜 | ベポタスチンベシル | タリオン® |
| 12歳〜 | ルパタジン | ルパフィン® |
| デスロラタジン | デザレックス® | |
| 成人 | ビラスチン | ビラノア® |
| エバスチン | エバステル® |
※オキサトミド(セルテクト® 鎮静性)は幼児以上で使用可能だったが、2018年8月で販売中止となった
- 1・2. アレジオン®・クラリチン®:3歳〜
- 3・4. ザイザル®・ザジテン®:6ヶ月〜
- 5. ジルテック®:2歳〜
過敏症以外の禁忌
- ザジテン®:てんかんまたはその既往
- ザイザル®:CCr<10mL/minの重度腎機能障害
- 参考:アトピー性皮膚炎診療ガイドライン 2021 日皮会誌:131(13), 2691-2777, 2021の表14(p2725-2726)
関連問題
選択問題31〜60は下記
-

-
令和1年度(2019年度) 皮膚科専門医試験 過去問 解答解説 選択問題31〜60
続きを見る